Будова атома: склад, моделі та роль у хімії й фізиці
Коли ми дивимось на світ навколо, нам важко повірити, що все складається з крихітних частинок, яких не побачиш навіть у звичайний мікроскоп. Та саме ці невидимі цеглинки — атоми — формують усе, що ми бачимо, відчуваємо і чим є ми самі.
Що таке атом
Атом — найменша частинка хімічного елемента, яка зберігає його властивості. Якщо взяти шматочок золота і поділити його навпіл, а потім ще раз і ще, то в певний момент ми отримаємо найменшу частинку, яка все ще буде золотом. Це і буде атом золота.
Атоми електронейтральні, бо містять однакову кількість позитивних і негативних зарядів. Розмір атома дуже малий — близько 0,1 нанометра. Щоб уявити цей розмір, подумайте про яблуко, збільшене до розміру Землі — тоді атоми в ньому будуть як звичайні яблука.
З чого складається атом
Атом має ядро і електронну оболонку, як планета із супутниками.
Ядро займає лише одну десятитисячну частину об’єму атома, але містить майже всю його масу. Воно складається з протонів і нейтронів. Протони мають позитивний заряд, а нейтрони — нейтральні. Кількість протонів визначає, який це хімічний елемент. Наприклад, атом водню має один протон, а атом кисню — вісім.
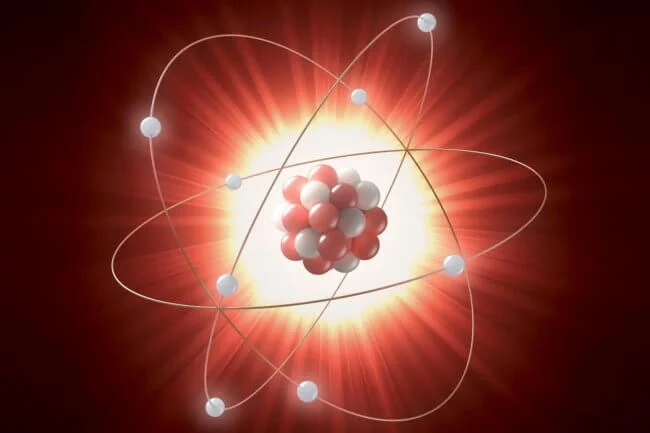 Навколо ядра рухаються електрони — легкі частинки з негативним зарядом. Вони формують електронну оболонку. Електрони літають навколо ядра, як метелики навколо лампи, але їх рух має чіткі правила. Вони розміщуються на різних енергетичних рівнях.
Навколо ядра рухаються електрони — легкі частинки з негативним зарядом. Вони формують електронну оболонку. Електрони літають навколо ядра, як метелики навколо лампи, але їх рух має чіткі правила. Вони розміщуються на різних енергетичних рівнях.
Взаємодія між частинами атома визначає його властивості. Ядро утримує електрони завдяки протилежним зарядам, як магніт притягує залізні ошурки.
Як уявляли атом вчені
З часом уявлення про будову атома змінювались.
Планетарна модель Резерфорда (1911) показала, що атом схожий на сонячну систему: в центрі — важке ядро, а навколо нього обертаються легкі електрони. Цей образ і досі часто використовують для пояснення будови атома дітям.
Модель Бора (1913) додала важливу деталь: електрони рухаються лише по певних орбітах, як поїзд по рейках. Коли електрон перестрибує з однієї орбіти на іншу, атом випромінює або поглинає енергію. Це пояснює, чому натрій в полум’ї дає жовте світло, а мідь — зелене.
Сучасна квантово-механічна модель описує електрони як хмаринки ймовірності. Ми не можемо точно сказати, де знаходиться електрон, але можемо визначити область, де його найімовірніше знайти. Ця модель нагадує розмиту фотографію швидкого автомобіля.
Ізотопи та іони
Ізотопи — це атоми одного елемента з різною кількістю нейтронів. Наприклад, звичайний водень має один протон без нейтронів, а важкий водень (дейтерій) — один протон і один нейтрон. Ізотопи мають схожі хімічні властивості, але різну масу. Ми використовуємо їх у медицині для діагностики хвороб та в археології для визначення віку знахідок.
Іони утворюються, коли атом втрачає або приєднує електрони. Якщо атом натрію віддає електрон, він стає позитивно зарядженим іоном. Коли атом хлору приймає електрон, він стає негативним іоном. Такі заряджені частинки притягуються одна до одної і утворюють кухонну сіль.
Чому важлива будова атома
Будова атома визначає хімічні властивості речовин. Елементи з подібною будовою зовнішньої електронної оболонки мають схожі властивості — це основа періодичної системи Менделєєва.
Розуміння будови атома дало нам ядерну енергію, сучасну медицину і електроніку. Без цих знань у нас не було б комп’ютерів, смартфонів, МРТ та багатьох ліків.
 Як відкривали атом
Як відкривали атом
Історія вивчення атома — це шлях від здогадок до точних знань. Ще у Стародавній Греції філософ Демокріт висловив думку про існування неподільних частинок. У 1803 році Джон Дальтон науково обґрунтував атомну теорію.
Справжній прорив стався в XX столітті. Ернест Резерфорд провів знаменитий дослід, в якому альфа-частинки пролітали крізь тонку золоту фольгу. Більшість частинок проходила, але деякі відбивались назад. Це було схоже на ситуацію, коли кинуті в пустелю тенісні м’ячі раптом повертаються назад — неочікувано і дивно. Так було відкрито атомне ядро.
Що ми знаємо сьогодні
Сучасні технології дозволяють нам не лише вивчати, але й керувати окремими атомами. За допомогою скануючого тунельного мікроскопа вчені можуть “побачити” атоми і навіть пересувати їх, ніби шашки на дошці.
Дослідження на Великому адронному колайдері розширюють наші знання про елементарні частинки. Ми вже знаємо, що протони і нейтрони складаються з ще менших частинок — кварків.
Атом — це цілий світ у мініатюрі, який ми продовжуємо вивчати і сьогодні. Від простих моделей до складних квантових теорій — наше розуміння атома постійно поглиблюється. Знання про будову атома змінили наш світ і відкрили двері до нових технологій.
Вивчаючи найменше, ми пізнаємо найбільше — від атома до Всесвіту. Продовжуйте цікавитись цією захоплюючою темою, і вона відкриє для вас багато нових таємниць природи.

Пишу про все, що надихає та змушує задуматися. Маю журналістську освіту та багато років досвіду у створенні пізнавальних матеріалів. Захоплююсь наукою, культурою та історіями успіху. Шукаю цікаве в усьому, аби ділитися знаннями, які допомагають відкривати нові горизонти, бачити красу світу та отримувати корисні поради для життя.

 Як відкривали атом
Як відкривали атом